
Bio-Tinte als Knorpelersatz
Das Projekt TriggerINK am DWI – Leibniz-Institut für Interaktive Materialien in Aachen strebt danach, körpereigenen Knorpel am beschädigten Gelenk mithilfe eines Stützgerüsts aus Bio-Tinte nachwachsen zu lassen. Die Neuentwicklung basiert auf dem Prinzip des 4D-Drucks. Die Werner Siemens-Stiftung unterstützt das innovative Vorhaben für die nächsten fünf Jahre.
Gelenkschmerzen zählen zu den häufigsten Gesundheitsproblemen unserer Zeit. Die Gründe dafür sind vielfältig, doch besonders oft leiden Menschen an Knorpelverschleiss (Arthrose) oder Meniskusschäden im Knie. Menisken und Knorpel übernehmen wichtige Aufgaben im Gelenk: Sie verteilen den durch Bewegung ausgeübten Druck und dämpfen Stösse ab. Sie ermöglichen es den Knochen, mit geringer Reibung und hoher Geschwindigkeit aneinander entlang zu gleiten. Und sie versorgen den Knochen mit Nährstoffen. Abgenutztes oder beschädigtes Knorpelgewebe wächst nicht von selbst nach. Zwar gibt es Verfahren wie die Knorpeltransplantation und einige Substanzen, die dem Aufbau des Gewebes helfen sollen, jedoch sind diese Eingriffe mit massiver Schädigung des gesunden Gewebes verbunden. Zudem ist der Erfolg der Eingriffe nicht garantiert.
3D-Druck mit zusätzlichen Funktionen
Abhilfe schaffen könnte das Projekt TriggerINK, das die Werner Siemens-Stiftung ab 2022 für einen Zeitraum von fünf Jahren mit insgesamt 10 Millionen Euro unterstützt. Dieses interdisziplinäre Forschungsprojekt am DWI – Leibniz-Institut für Interaktive Materialien in Aachen zielt darauf ab, eine visionäre Methode zur Knorpel-Regenerierung zu entwickeln. TriggerINK bedient sich des neuartigen Prinzips des 4D-Drucks. Dabei handelt es sich um eine Weiterentwicklung des 3D-Drucks, bei dem ein Material Schicht für Schicht zu einer dreidimensionalen Struktur gedruckt wird. Als vierte Dimension kommt beim 4D-Druck die Zeit ins Spiel: Die 3D-Struktur ist so konstruiert, dass sie durch einen äusseren Auslöser wie beispielsweise Wärme, Vibration oder Schall nachträglich bewegt oder verändert werden kann.
Fachwissen aus vielen Disziplinen
Geleitet wird das Vorhaben von Laura De Laporte, Mitglied der wissenschaftlichen Leitung des DWI - Leibniz-Instituts für Interaktive Materialien und Professorin für Advanced Materials and Biomedicine an der Rheinisch-Westfälischen Technischen Hochschule (RWTH) Aachen. Es ist ein Paradebeispiel moderner Forschungszusammenarbeit: Erst durch die Bündelung der Kompetenzen verschiedener Fachrichtungen wird es realisierbar. Mit Laura De Laporte und ihrer Expertise in der Entwicklung biomedizinischer Materialien kommen insgesamt vier führende Wissenschaftler ihres Feldes zusammen: Die Kollegen Stefan Hecht (3D-Druck durch Licht), Andreas Herrmann (Wirkstoff-Freisetzung durch Ultraschall) und Matthias Wessling (technische Umsetzung des Verfahrens) machen das Team komplett. «Dass wir dieses unterschiedliche Wissen hier in Aachen unter einem Dach zusammenbringen, ist eine grosse Besonderheit und gleichzeitig Stärke für das Projekt», sagt Laura De Laporte. Darüber hinaus begleitet und berät ein Team externer Experten aus den Bereichen Medizin und Zellbiologie das Projekt.
Fein gesteuertes Gewebewachstum
Bei TriggerINK, so der Plan der Forschenden, wird eine solche 4D-Struktur direkt in der Wunde beziehungsweise im betroffenen Gelenk gedruckt. Der anvisierte Behandlungs- und Heilungsprozess beinhaltet die folgenden sechs Schritte:
-
Auf den noch bestehenden, gesäuberten Knorpel wird eine dünne Biopolymer-Schicht gesprayt. Sie sorgt für eine feste Haftung und dafür, dass das körpereigene Knorpelgewebe in das nun folgende künstliche Konstrukt aus dem 3D-Drucker hineinwachsen kann.
-
Schicht für Schicht druckt ein 3D-Drucker die eigentliche Bio-Tinte in die Wunde. Sie besteht aus einer gelatineartigen Substanz, einem sogenannten biologisch abbaubaren Hydro-Gel. Während des Drucks werden die Schichten immer wieder mit Licht von aussen bestrahlt. Das verändert die chemische Struktur der Bio-Tinte und verstärkt die Verbindung zwischen den einzelnen Schichten. So bildet sich nach und nach ein Stützgerüst mit Poren, durch die das körpereigene Knorpelgewebe nachwachsen kann.
-
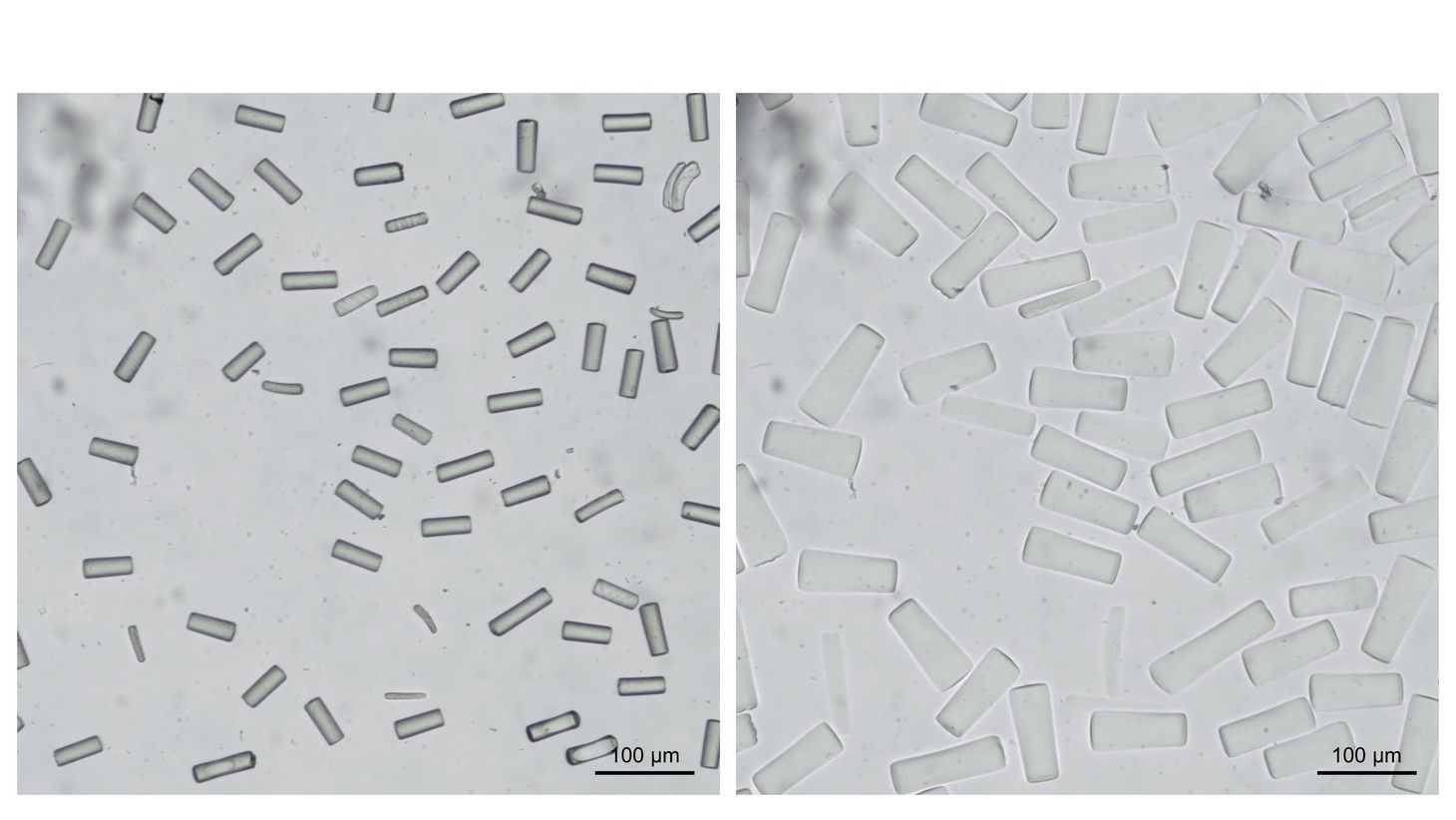
In die Bio-Tinte integriert sind unter anderem winzige Gel-Stäbchen, die magnetische Partikel enthalten. Bereits während das Stützgerüst gedruckt wird, werden sie mittels eines schwachen externen Magnetfelds ausgerichtet. Dadurch wird gewährleistet, dass die das Zellwachstum leitende Mikrostruktur eine bestimmte Richtung aufweist und das Knorpelgewebe somit in die gewünschte Richtung wächst.
-
Ebenfalls in der Bio-Tinte enthalten sind Wachstumsfaktoren und Nährstoffe. Bei Bedarf – zum Beispiel bei grösseren Wunden – werden sie durch Ultraschall freigesetzt, worauf sie den Wachstumsprozess des Knorpelgewebes fördern.
-
Nach einem medizinischen Eingriff sollten Gelenke und Gewebe möglichst rasch bewegt werden, um den Heilungsprozess zu beschleunigen. TriggerINK setzt auch dabei auf externe Impulse: Zum richtigen Zeitpunkt wird das sich entwickelnde Knorpelgewebe durch Licht- und Wärmeimpulse in kleinste Bewegungen versetzt – ein Vorgang, den die Forschenden «In-vivo-Gym» nennen.
-
Zum Schluss, wenn der körpereigene Knorpel nachgewachsen ist, baut sich das Hilfsgerüst aus der Bio-Tinte von selbst ab. Auch dieser Vorgang kann mittels äusserer Impulse beschleunigt werden.
Auch für andere Gewebe geeignet?
Funktioniert dieses neuartige und innovative Prinzip, verspricht es ganz neue Möglichkeiten in der Knorpelersatz-Therapie. Denn dass sich ein Knorpel oder auch ein Meniskus zielgenau wiederherstellen lässt, ist mit heutigen Ansätzen undenkbar. «Zudem wäre das Drucken des Stützgerüsts direkt ins Gelenk ein minimalinvasiver Eingriff», erklärt Stefan Hecht. «Wir müssen nichts herausfräsen oder herausschneiden.» Und vielleicht noch viel wichtiger: Die Technik der Aachener Forschenden hat ein Potenzial, das weit über Gelenkschmerzen hinausgeht. «Knorpel ist ein relativ einfach aufgebautes Gewebe. Deshalb konzentrieren wir uns in dem Projekt darauf», sagt Matthias Wessling. Die Technologie könne aber auch für andere beschädigte Gewebe weiterentwickelt werden. Beispiele dafür sind die Hornhaut des Auges, Sehnen oder Bandscheiben, Muskeln oder Nerven.
Vollgepackte Bio-Tinte
Es sei ein äusserst ambitioniertes Projekt, bei dem es vielerlei Herausforderungen zu meistern gelte, räumt das Forscherteam ein. Eine der grössten sieht Andreas Herrmann in der Herstellung der Bio-Tinte. Sie muss diverse Inhaltsstoffe enthalten, die alle voneinander abhängen und miteinander in Wechselwirkung stehen. Und sie funktioniert nur als Ganzes. Deshalb werde es nicht möglich sein, die Bio-Tinte Schritt für Schritt zu entwickeln, erklärt Andreas Herrmann. «Wir müssen viele verschiedene Inhaltsstoffe in ein und dieselbe Substanz packen – dass diese alle miteinander kompatibel sind, ist eine der zentralen Aufgaben, an der wir arbeiten.» Jede einzelne Komponente parallel zu entwickeln und in die Tinte einzubringen, ist schon eine Neuheit an sich. Doch, dass die einzelnen Komponenten auch in Kombination wie geplant ihre individuelle Funktion erfüllen, werde die grösste Herausforderung.
Ein neues Labor
Eine agile Organisation soll das Projekt rasch voranbringen. Bereits ab 2024 planen die Forschenden Tests in Versuchstieren. Zudem wollen das DWI – Leibniz-Institut für Interaktive Materialien und die RWTH Aachen noch dieses Jahr ein gemeinsames Labor namens «first in Translation» (fiT) eröffnen, das unter anderem mit insgesamt 425 Quadratmeter grossen Reinräumen ausgestattet ist. Es diene dazu, die Lücke zwischen präklinischer und klinischer Forschung zu schliessen, erklärt Laura De Laporte. «Denn, um zur Anwendungsreife gebracht zu werden, muss die Bio-Tinte irgendwann in grösserem Massstab hergestellt und unser Verfahren in der Klinik überprüft werden.» Immer mit dem Ziel, dereinst die Gelenkschmerzen von Millionen Menschen zu lindern.

Zahlen und Fakten
Mittel der Werner Siemens-Stiftung
10 Mio. Euro für 5 Jahre
Projektdauer
2022–2026
Projektleitung
Prof. Dr.-Ing. Laura De Laporte, Mitglied der wissenschaftlichen Leitung des DWI - Leibniz-Institut für Interaktive Materialien und Professorin für Advanced Materials and Biomedicine an der RWTH Aachen
Prof. Stefan Hecht, Ph.D., Wissenschaftlicher Direktor des DWI - Leibniz-Institut für Interaktive Materialien und Professor für Makromolekulare Chemie an der RWTH Aachen
Prof. Dr. Andreas Herrmann, stellvertretender Wissenschaftlicher Direktor des DWI - Leibniz-Institut für Interaktive Materialien und Professor für Makromolekulare Materialien und Systeme an der RWTH Aachen
Prof. Dr.-Ing. Matthias Wessling, Mitglied der wissenschaftlichen Leitung des DWI - Leibniz-Institut für Interaktive Materialien und Professor für Chemische Verfahrenstechnik an der RWTH Aachen
Projektpartner und Berater
Prof. Dr. med. Dr. rer. nat. Rebekka Schneider-Kramann, Professorin am Institut für Biomedical Engineering an der RWTH Aachen und dem Universitätsklinikum Aachen
Prof. Dr. med. Fabian Kiessling, Professor für experimentelle molekulare Bildgebung an der RWTH Aachen und dem Universitätsklinikum Aachen
Prof. Dr. Frank Luyten, Professor für Rheumatologie, Abteilung für Muskel-Skelett-Wissenschaften an den Universitätskliniken Leuven
Prof. Dr. Peter Verdonk, Professor und Orthopädischer Chirurg im Bereich der Knie-Rekonstruktion an der Universität Antwerpen



